Diferenciación de núcleos según la intensidad de la señal#
Una tarea común en el análisis de bioimágenes es diferenciar células según su expresión de señal. En este ejemplo, tomamos una imagen de dos canales de núcleos que expresan Cy3 y eGFP. Visualmente, podemos ver fácilmente que algunos núcleos que expresan Cy3 también expresan eGFP, mientras que otros no. Este notebook demuestra cómo diferenciar núcleos segmentados en un canal según la intensidad en el otro canal.
import pyclesperanto_prototype as cle
import numpy as np
from skimage.io import imread, imshow
import matplotlib.pyplot as plt
import pandas as pd
cle.get_device()
<Intel(R) Iris(R) Xe Graphics on Platform: Intel(R) OpenCL HD Graphics (1 refs)>
Estamos utilizando un conjunto de datos publicado por Heriche et al. con licencia CC BY 4.0 disponible en el Image Data Resource.
# load file
raw_image = imread('../../data/plate1_1_013 [Well 5, Field 1 (Spot 5)].png')
# visualize
imshow(raw_image)
<matplotlib.image.AxesImage at 0x1dac72d7c40>
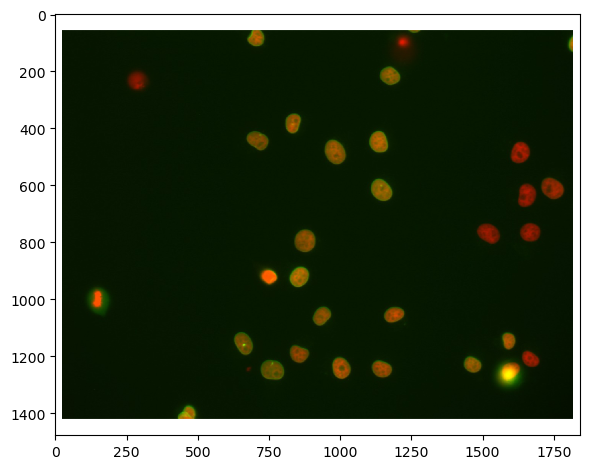
Primero, necesitamos separar los canales (leer más). Después de eso, realmente podemos ver que no todas las células marcadas con Cy3 (canal 0) también están marcadas con eGFP (canal 1):
# extract channels
channel_cy3 = raw_image[...,0]
channel_egfp = raw_image[...,1]
# visualize
fig, axs = plt.subplots(1, 2, figsize=(15,15))
axs[0].imshow(channel_cy3, cmap='gray')
axs[1].imshow(channel_egfp, cmap='gray')
<matplotlib.image.AxesImage at 0x1dac7328970>
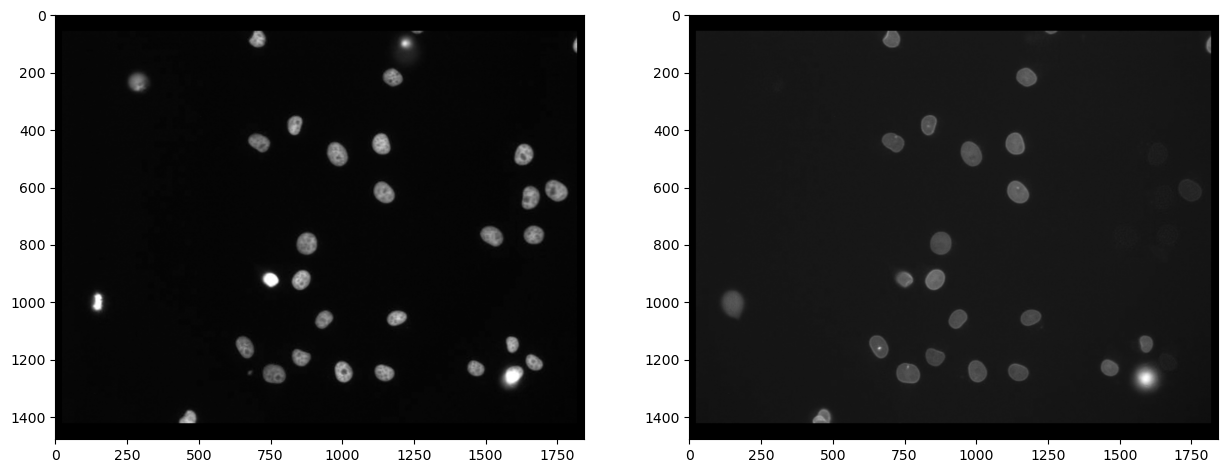
Segmentación de núcleos#
Como la tinción marca los núcleos en el canal Cy3, es razonable segmentar los núcleos en este canal y después medir la intensidad en el otro canal. Usamos Voronoi-Otsu-Labeling para la segmentación porque es un enfoque rápido y directo.
# segmentation
nuclei_cy3 = cle.voronoi_otsu_labeling(channel_cy3, spot_sigma=20)
# visualize
fig, axs = plt.subplots(1, 2, figsize=(15,15))
cle.imshow(channel_cy3, plot=axs[0], color_map="gray")
cle.imshow(nuclei_cy3, plot=axs[1], labels=True)
C:\Users\rober\miniconda3\envs\bio39\lib\site-packages\pyclesperanto_prototype\_tier9\_imshow.py:46: UserWarning: The imshow parameter color_map is deprecated. Use colormap instead.
warnings.warn("The imshow parameter color_map is deprecated. Use colormap instead.")
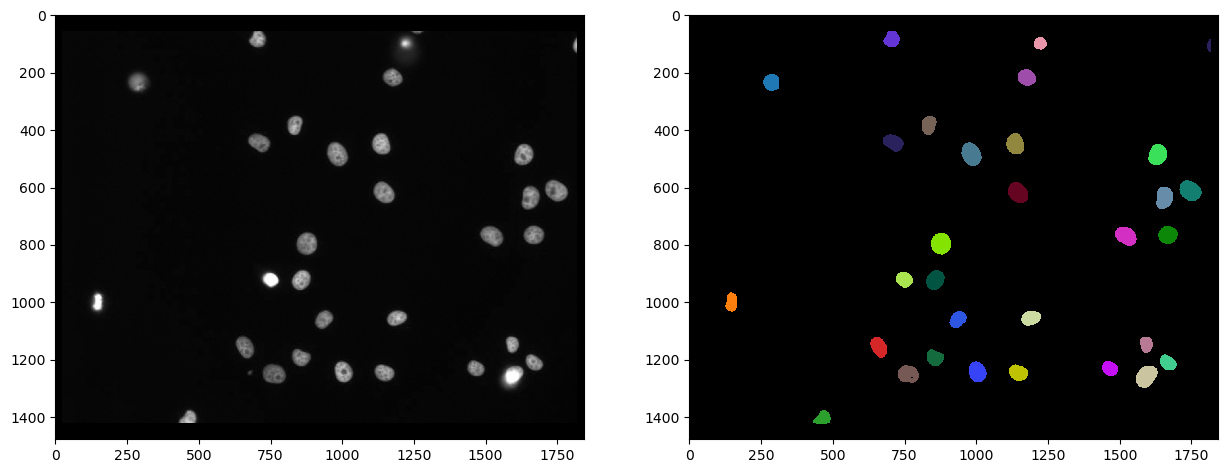
En primer lugar, podemos medir la intensidad en el segundo canal, marcado con eGFP y visualizar esa medición en una imagen paramétrica. En tal imagen paramétrica, todos los píxeles dentro de un núcleo tienen el mismo valor, en este caso la intensidad media promedio de la célula.
intensity_map = cle.mean_intensity_map(channel_egfp, nuclei_cy3)
# visualize
fig, axs = plt.subplots(1, 2, figsize=(15,15))
cle.imshow(channel_egfp, plot=axs[0], color_map="gray")
cle.imshow(intensity_map, plot=axs[1], color_map="gray")
C:\Users\rober\miniconda3\envs\bio39\lib\site-packages\pyclesperanto_prototype\_tier9\_imshow.py:46: UserWarning: The imshow parameter color_map is deprecated. Use colormap instead.
warnings.warn("The imshow parameter color_map is deprecated. Use colormap instead.")
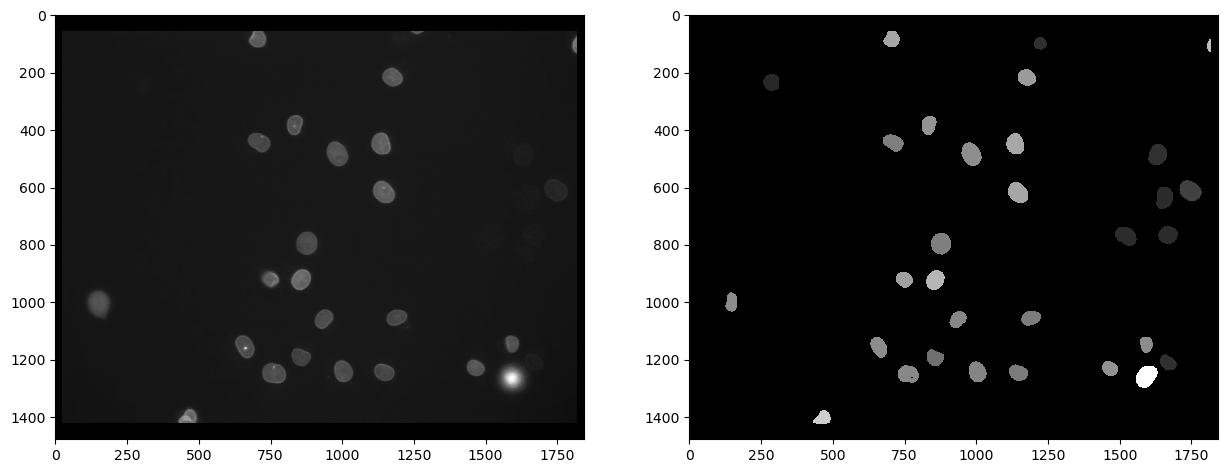
A partir de tal imagen paramétrica, podemos recuperar los valores de intensidad y obtenerlos en un vector. El primer elemento de esta lista tiene valor 0 y corresponde a la intensidad del fondo, que es 0 en la imagen paramétrica.
intensity_vector = cle.read_intensities_from_map(nuclei_cy3, intensity_map)
intensity_vector
cle.array([[ 0. 80.875854 23.529799 118.17817 80.730255 95.55177 72.84752 92.34759 78.84362 85.400444 105.108025 65.06639 73.69295 77.40091 81.48371 77.12868 96.58209 95.94536 70.883995 89.70502 72.01046 27.257877 84.460075 25.49711 80.69057 147.49736 28.112642 25.167627 28.448263 25.31705 38.072815 108.81613 ]], dtype=float32)
Por cierto, también hay una forma alternativa de llegar a las intensidades medias directamente, midiendo todas las propiedades de los núcleos, incluyendo posición y forma. Las estadísticas pueden procesarse adicionalmente como un DataFrame de pandas.
statistics = cle.statistics_of_background_and_labelled_pixels(channel_egfp, nuclei_cy3)
statistics_df = pd.DataFrame(statistics)
statistics_df.head()
| label | original_label | bbox_min_x | bbox_min_y | bbox_min_z | bbox_max_x | bbox_max_y | bbox_max_z | bbox_width | bbox_height | ... | centroid_z | sum_distance_to_centroid | mean_distance_to_centroid | sum_distance_to_mass_center | mean_distance_to_mass_center | standard_deviation_intensity | max_distance_to_centroid | max_distance_to_mass_center | mean_max_distance_to_centroid_ratio | mean_max_distance_to_mass_center_ratio | |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 0 | 1 | 0 | 0.0 | 0.0 | 0.0 | 1841.0 | 1477.0 | 0.0 | 1842.0 | 1478.0 | ... | 0.0 | 1.683849e+09 | 640.648682 | 1.683884e+09 | 640.661682 | 8.487288 | 1187.033203 | 1187.743164 | 1.852861 | 1.853932 |
| 1 | 2 | 1 | 127.0 | 967.0 | 0.0 | 167.0 | 1033.0 | 0.0 | 41.0 | 67.0 | ... | 0.0 | 4.128044e+04 | 18.704323 | 4.128327e+04 | 18.705606 | 4.734930 | 34.280727 | 34.338104 | 1.832770 | 1.835712 |
| 2 | 3 | 2 | 259.0 | 205.0 | 0.0 | 314.0 | 265.0 | 0.0 | 56.0 | 61.0 | ... | 0.0 | 5.392080e+04 | 19.715099 | 5.393993e+04 | 19.722092 | 1.663603 | 32.079941 | 31.469477 | 1.627176 | 1.595646 |
| 3 | 4 | 3 | 432.0 | 1377.0 | 0.0 | 492.0 | 1423.0 | 0.0 | 61.0 | 47.0 | ... | 0.0 | 3.630314e+04 | 17.769527 | 3.636823e+04 | 17.801388 | 24.842560 | 36.856213 | 36.085457 | 2.074125 | 2.027115 |
| 4 | 5 | 4 | 631.0 | 1123.0 | 0.0 | 690.0 | 1194.0 | 0.0 | 60.0 | 72.0 | ... | 0.0 | 6.753254e+04 | 21.686750 | 6.755171e+04 | 21.692907 | 17.358543 | 38.805695 | 38.417568 | 1.789373 | 1.770974 |
5 rows × 37 columns
El vector de intensidad puede entonces recuperarse de las estadísticas tabulares. Nota: En este caso, la intensidad del fondo no es 0, porque la estábamos leyendo directamente de la imagen original.
intensity_vector2 = statistics['mean_intensity']
intensity_vector2
array([ 20.829758, 80.875854, 23.529799, 118.17817 , 80.730255,
95.55177 , 72.84752 , 92.34759 , 78.84362 , 85.400444,
105.108025, 65.06639 , 73.69295 , 77.40091 , 81.48371 ,
77.12868 , 96.58209 , 95.94536 , 70.883995, 89.70502 ,
72.01046 , 27.257877, 84.460075, 25.49711 , 80.69057 ,
147.49736 , 28.112642, 25.167627, 28.448263, 25.31705 ,
38.072815, 108.81613 ], dtype=float32)
Para obtener una visión general de la medición de intensidad media, podemos usar matplotlib para trazar un histograma. Ignoramos el primer elemento, porque corresponde a la intensidad del fondo.
plt.hist(intensity_vector2[1:])
(array([ 7., 1., 0., 4., 10., 5., 2., 1., 0., 1.]),
array([ 23.52979851, 35.92655563, 48.32331085, 60.72006607,
73.11682129, 85.51358032, 97.91033936, 110.30709076,
122.70384979, 135.1006012 , 147.49736023]),
<BarContainer object of 10 artists>)
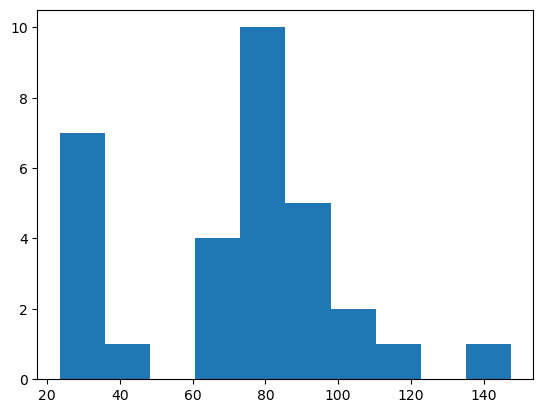
A partir de tal histograma, podríamos concluir que los objetos con intensidad superior a 50 son positivos.
Selección de etiquetas por encima de un umbral de intensidad dado#
A continuación, generamos una nueva imagen de etiquetas con los núcleos que tienen una intensidad > 50. Nota, todos los pasos anteriores para extraer el vector de intensidad no son necesarios para esto. Solo lo hicimos para tener una idea de un buen umbral de intensidad.
La siguiente imagen de etiquetas muestra los núcleos segmentados en el canal Cy3 que tienen una alta intensidad en el canal eGFP.
intensity_threshold = 50
nuclei_with_high_intensity_egfg = cle.exclude_labels_with_map_values_within_range(intensity_map, nuclei_cy3, maximum_value_range=intensity_threshold)
intensity_map = cle.mean_intensity_map(channel_egfp, nuclei_cy3)
# visualize
fig, axs = plt.subplots(1, 2, figsize=(15,15))
cle.imshow(channel_egfp, plot=axs[0], color_map="gray")
cle.imshow(nuclei_with_high_intensity_egfg, plot=axs[1], labels=True)
C:\Users\rober\miniconda3\envs\bio39\lib\site-packages\pyclesperanto_prototype\_tier9\_imshow.py:46: UserWarning: The imshow parameter color_map is deprecated. Use colormap instead.
warnings.warn("The imshow parameter color_map is deprecated. Use colormap instead.")
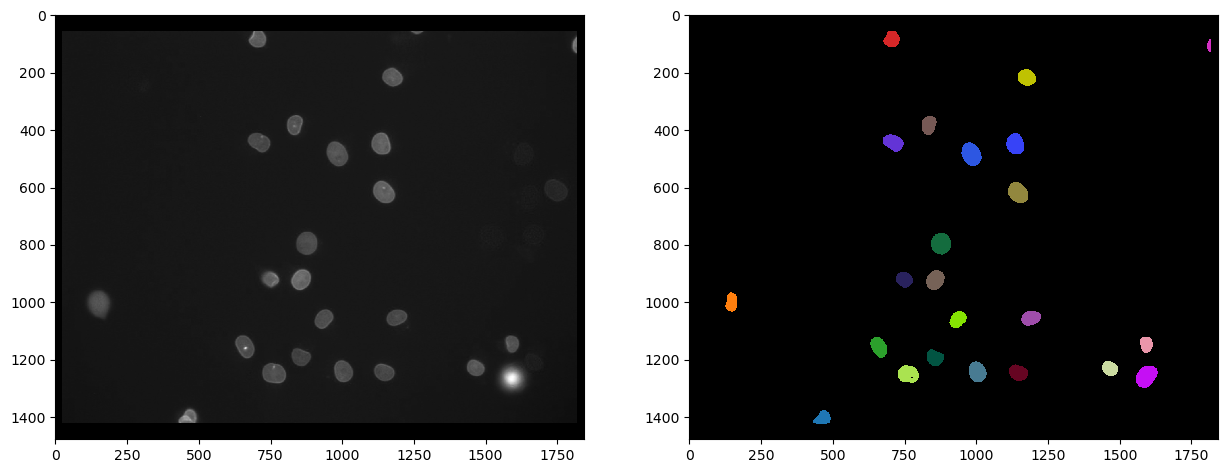
Y también podemos contarlos determinando la intensidad máxima en la imagen de etiquetas:
number_of_double_positives = nuclei_with_high_intensity_egfg.max()
print("Número de núcleos Cy3 que también expresan eGFP", number_of_double_positives)
Number of Cy3 nuclei that also express eGFP 23.0
Referencias#
Algunas de las funciones que usamos pueden ser poco comunes. Por lo tanto, podemos agregar su documentación como referencia.
print(cle.voronoi_otsu_labeling.__doc__)
Labels objects directly from grey-value images.
The two sigma parameters allow tuning the segmentation result. Under the hood,
this filter applies two Gaussian blurs, spot detection, Otsu-thresholding [2] and Voronoi-labeling [3]. The
thresholded binary image is flooded using the Voronoi tesselation approach starting from the found local maxima.
Notes
-----
* This operation assumes input images are isotropic.
Parameters
----------
source : Image
Input grey-value image
label_image_destination : Image, optional
Output image
spot_sigma : float, optional
controls how close detected cells can be
outline_sigma : float, optional
controls how precise segmented objects are outlined.
Returns
-------
label_image_destination
Examples
--------
>>> import pyclesperanto_prototype as cle
>>> cle.voronoi_otsu_labeling(source, label_image_destination, 10, 2)
References
----------
.. [1] https://clij.github.io/clij2-docs/reference_voronoiOtsuLabeling
.. [2] https://ieeexplore.ieee.org/document/4310076
.. [3] https://en.wikipedia.org/wiki/Voronoi_diagram
print(cle.mean_intensity_map.__doc__)
Takes an image and a corresponding label map, determines the mean
intensity per label and replaces every label with the that number.
This results in a parametric image expressing mean object intensity.
Parameters
----------
source : Image
label_map : Image
destination : Image, optional
Returns
-------
destination
References
----------
.. [1] https://clij.github.io/clij2-docs/reference_meanIntensityMap
print(cle.read_intensities_from_map.__doc__)
Takes a label image and a parametric image to read parametric values from the labels positions.
The read intensity values are stored in a new vector.
Note: This will only work if all labels have number of voxels == 1 or if all pixels in each label have the same value.
Parameters
----------
labels: Image
map_image: Image
values_destination: Image, optional
1d vector with length == number of labels + 1
Returns
-------
values_destination, Image:
vector of intensity values with 0th element corresponding to background and subsequent entries corresponding to
the intensity in the given labeled object
print(cle.statistics_of_background_and_labelled_pixels.__doc__)
Determines bounding box, area (in pixels/voxels), min, max and mean
intensity of background and labelled objects in a label map and corresponding
pixels in the original image.
Instead of a label map, you can also use a binary image as a binary image is a
label map with just one label.
This method is executed on the CPU and not on the GPU/OpenCL device.
Parameters
----------
source : Image
labelmap : Image
Returns
-------
Dictionary of measurements
References
----------
.. [1] https://clij.github.io/clij2-docs/reference_statisticsOfBackgroundAndLabelledPixels
print(cle.exclude_labels_with_map_values_within_range.__doc__)
This operation removes labels from a labelmap and renumbers the
remaining labels.
Notes
-----
* Values of all pixels in a label each must be identical.
Parameters
----------
values_map : Image
label_map_input : Image
label_map_destination : Image, optional
minimum_value_range : Number, optional
maximum_value_range : Number, optional
Returns
-------
label_map_destination
References
----------
.. [1] https://clij.github.io/clij2-docs/reference_excludeLabelsWithValuesWithinRange
